Descartan que brote de bacteria Klebsiella oxytoca se haya originado en empresa farmacéutica
Hasta el momento, han fallecido 13 menores en cuatro hospitales del Estado de México
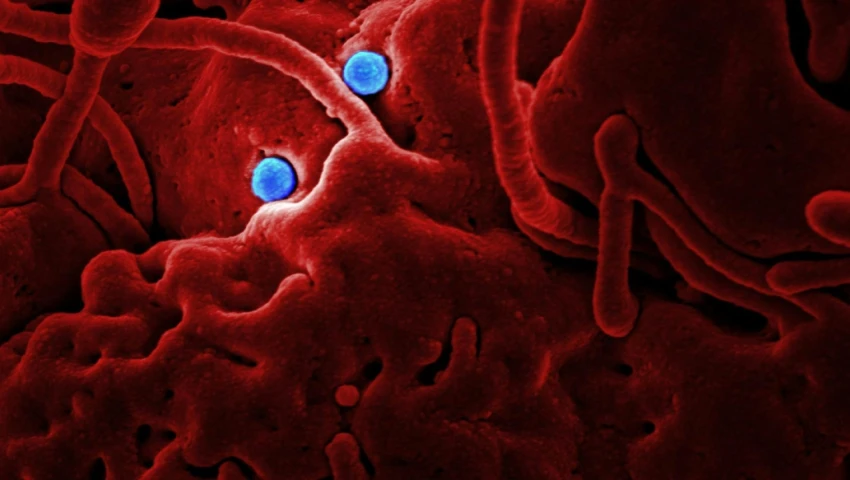
A principios de diciembre se dio a conocer que un brote de Infección del Torrente Sanguíneo (ITS) causado por la bacteria Klebsiella oxytoca multidrogo resistente se registró en el Estado de México, el cual ha cobrado la vida de 13 menores en cuatro hospitales. Aunque la Secretaría de Salud, consideró que dicho brote podría estar relacionado con la contaminación de soluciones intravenosas utilizadas en los tratamientos, se confirmó que no es así.
Mediante un comunicado emitido por la dependencia federal este 7 de diciembre, se informó que a la Comisión Federal para la Protección contra Riesgos Sanitarios, Cofepris, realizó una inspección en la central de mezclas donde se produjeron estas nutriciones paraenterales, “concluyendo que no se encontraron hallazgos críticos en dichas instalaciones”.
Antes de los recientes hallazgos, Cofepris emitió una alerta sanitaria para la inmovilización preventiva de los lotes de nutrición parenteral producidos por la empresa SAFE, filial de PISA, a partir del 21 de noviembre, hasta que se tenga información concluyente que incluya el análisis de las materias primas,
La sospecha descartada
El brote había sido vinculado a las soluciones de Nutrición Parenteral Total (NPT) de la empresa SAFE, así como con los insumos empleados para su aplicación, pero se ha descartado que ese sea el caso.
Sin embargo, las autoridades no habían descartado otras posibles fuentes e iniciaron un análisis exhaustivo para identificar la causa. La Secretaría de Salud asegura que se está llevando a cabo un monitoreo constante para prevenir nuevos brotes en otras regiones.
De los 20 casos detectados, 15 han sido confirmados con la presencia de la bacteria Klebsiella oxytoca MDR, mientras que cuatro permanecen como casos probables y uno ha sido descartado.
¿Qué es SAFE?
SAFE, es una división de PiSA Farmacéutica, es conocida por ser la primera empresa en México en establecer una línea completa para nutrición artificial parenteral en 1988, lo que marcó un hito en el ámbito médico de Latinoamérica. Esta división está especializada en soluciones de nutrición parenteral total (NPT), las cuales se administran por vía intravenosa a pacientes que no pueden ingerir o absorber nutrientes de forma convencional.
PiSA Farmacéutica, fundada en 1945 y con sede en Guadalajara, Jalisco, es líder en la industria farmacéutica mexicana. Cuenta con más de 14 plantas de producción, 20,000 colaboradores, y 17 líneas de especialidad médica. Entre sus productos más reconocidos se encuentran Electrolit y una amplia gama de soluciones médicas avanzadas.
En 2019, la empresa PiSA habría declarado un desabasto ficticio del medicamento metotrexato, utilizado para tratar el cáncer infantil, sin embargo, la empresa sí contaba con esta medicina.








